Tableau périodique des éléments : Différence entre versions
| (63 révisions intermédiaires par 3 utilisateurs non affichées) | |||
| Ligne 1 : | Ligne 1 : | ||
| − | <b> | + | *Pendant l'[[Antiquité]], on considérait <b>les éléments</b> différemment : les corps étaient classés en solides, liquides et vapeurs et selon leur couleur, et leur interaction suivant des notions de sympathie et d'antipathie. Cette philosophie reposait sur la théorie des quatre éléments (le feu, l’eau, la terre et l’air) d'[[Aristote]] reprise par [[Platon]]. (Voir l'histoire de la [[chimie]]). |
| − | + | *<b>[[Origine des éléments]]</b> (Suivre le lien), à noter que les tout premiers éléments formés naturellement ([[Big Bang]]) se retrouvent en haut du tableau (ligne 1 : [[hydrogène]] et [[hélium]]), et les éléments synthétisés par l'homme ([[éléments synthétiques]]), sont en bas du tableau (voir le tableau ci-dessous). | |
| + | *<b>Les [[éléments]] chimiques</b> sont une catégorie d'[[atome]]s ayants en commun le même nombre de protons dans leur noyau atomique. Un atome est un assemblage de protons, de charge positive, et de neutrons, de charge nulle, le tout entouré d'électrons de charge électrique négative. Les [[atome]]s peuvent se combiner de façons très variables. Sous forme pure, ils peuvent se présenter notamment : comme des [[atome]]s séparés, comme des molécules (comprenant plusieurs atomes d'un même élément), comme des solides cristallins (ou amorphes). | ||
| + | <center>[[Image:Atome_bis.jpg]]</center> | ||
| + | |||
| + | *<b>Élément natif</b> (adj.) du latin <em>nativus</em>, naturel : Qualifie les [[éléments]] chimiques métalliques qui se trouvent dans la nature à l'état pur ([[or]], [[argent]], [[cuivre]], [[fer]], [[chrome]], [[aluminium]], [[mercure]], etc.). Certains des éléments natifs peuvent se combiner et constituer des " alliages " ou des " amalgames " naturels… | ||
| + | |||
| + | *<b>Tableau périodique des éléments</b> : ou tableau de [[Mendeleïev]], regroupe tous les éléments avec, leur numéro atomique, la [[masse atomique]], le nom, le symbole... Ce tableau est dit périodique car tous les éléments situés dans une même colonne (de 1 à 18), présentent des propriétés chimiques proches. Par exemple : dans la colonne 1, le [[lithium]] (Li) et le [[sodium]] (Na) ont un comportement chimique proche. L'explication de ce comportement repose sur le fait que le nombre d'électrons de leur couche de valence (tous les électrons présents en plus de la configuration du dernier gaz rare) est identique. Li et Na ont un seul électron de valence. C'est cet électron externe qui est disponible pour les réactions chimiques. D'où des propriétés chimiques proches et par conséquent leur regroupement dans une même famille d'éléments. | ||
| + | |||
| + | |||
| + | *Les éléments, ([[métaux]], à gauche du tableau et non métaux, à droite du tableau) sont regroupés en dix séries chimiques aux propriétés physicochimiques homogènes : | ||
| + | **Série des [[métaux alcalins]], | ||
| + | **Série des [[métaux alcalino-terreux]], | ||
| + | **Série des [[lanthanides]] : Z = 57 à 71, | ||
| + | **Série des [[actinides]] : Z = 89 à 103, | ||
| + | **Série des [[métaux de transition]] (colonnes 3 à 12), | ||
| + | **Série des [[métaux pauvres]] entre les métalloïdes et les métaux de transition (Al, Ga, In, Sn, Tl, Pb, Bi), | ||
| + | **Série des [[métalloïdes]] : entre les deux précédents (B, Si, Ge, As, Sb, Te, Po), | ||
| + | **Série des [[non-métaux]] à droite du tableau : | ||
| + | **Série des [[halogènes]] : colonne 17, | ||
| + | **Série des [[gaz nobles]] : colonne 18. | ||
| + | *Chaque série correspondant à une couleur du tableau. | ||
| + | <hr> | ||
| + | <center>[[Image:Tableau_%C3%A9l%C3%A9ments_1bis.jpg]]</center><br> | ||
| + | <b><font color="green">Pour voir le tableau en plus grand, voir :</font> [[Le tableau des éléments]]</b><br> | ||
| + | Une autre version (plus ancienne) du tableau périodique des éléments se trouve à : [[FORMULES CHIMIQUES]] et à [[Mendeleïev]]. | ||
| + | <hr> | ||
| + | |||
| + | *Les éléments sont aussi placés dans des groupes, dont chacun a des propriétés bien distinctes de celles des groupes voisins. On distingue 18 groupes : | ||
| + | :groupe 1 des métaux alcalins | ||
| + | :groupe 2 des métaux alcalino-terreux | ||
| + | :groupe 14 des cristallogènes | ||
| + | :groupe 15 des pnictogènes | ||
| + | :groupe 16 des chalcogènes | ||
| + | :groupe 17 des halogènes | ||
| + | :groupe 18 des gaz rares | ||
| + | :+ groupe des lanthanides et actinides | ||
| + | :+ groupe du platine (ruthénium, rhodium, osmium, iridium et platine). | ||
| + | :+ les [[terres rares]] | ||
| + | |||
| + | <center> | ||
| + | {| class="wikitable"|width=100%| | ||
| + | <hr> | ||
| + | |+<b><font color="greeen"><big>liste de tous les éléments:</big></font></b> | ||
| + | <br><br> | ||
| + | N° atomique, nom, symbole chimique. | ||
| + | <hr> | ||
| + | |width:25%| | ||
| + | | | ||
| + | *1 [[Hydrogène]] H | ||
| + | *2 [[Hélium]] He | ||
| + | *3 [[Lithium]] Li | ||
| + | *4 [[Béryllium]] Be | ||
| + | *5 [[Bore]] B | ||
| + | *6 [[Carbone]] C | ||
| + | *7 [[Azote]] N | ||
| + | *8 [[Oxygène]] O | ||
| + | *9 [[Fluor]] F | ||
| + | *11 [[Sodium]] Na | ||
| + | *12 [[Magnésium]] Mg | ||
| + | *13 [[Aluminium]] Al | ||
| + | *14 [[Silicium]] Si | ||
| + | *15 [[Phosphore]] P | ||
| + | *16 [[Soufre]] S | ||
| + | *17 [[Chlore]] Cl | ||
| + | *18 [[Argon]] Ar | ||
| + | *19 [[Potassium]] K | ||
| + | *20 [[Calcium]] Ca | ||
| + | *21 [[Scandium]] Sc | ||
| + | *22 [[Titane]] Ti | ||
| + | *23 [[Vanadium]] V | ||
| + | *24 [[Chrome]] Cr | ||
| + | *25 [[Manganèse]] Mn | ||
| + | *26 [[Fer]] Fe | ||
| + | *27 [[Cobalt]] Co | ||
| + | *28 [[Nickel]] Ni | ||
| + | *29 [[Cuivre]] Cu | ||
| + | |width:25%| | ||
| + | | | ||
| + | *30 [[Zinc]] Zn | ||
| + | *32 [[Germanium]] Ge | ||
| + | *33 [[Arsenic]] As | ||
| + | *34 [[Sélénium]] Se | ||
| + | *35 [[Brome]] Br | ||
| + | *36 [[Krypton]] Kr | ||
| + | *37 [[Rubidium]] Rb | ||
| + | *38 [[Strontium]] Sr | ||
| + | *39 [[Yttrium]] Y | ||
| + | *40 [[Zirconium]] Zr | ||
| + | *41 [[Niobium]] Nb | ||
| + | *42 [[Molybdène]] Mo | ||
| + | *43 [[Technétium]] Tc | ||
| + | *44 [[Ruthénium]] Ru | ||
| + | *45 [[Rhodium]] Rh | ||
| + | *46 [[Palladium]] Pd | ||
| + | *47 [[Argent]] Ag | ||
| + | *48 [[Cadmium]] Cd | ||
| + | *49 [[Indium]] In | ||
| + | *50 [[Étain]] Sn | ||
| + | *51 [[Antimoine]] Sb | ||
| + | *52 [[Tellure]] Te | ||
| + | *53 [[Iode]] I | ||
| + | *54 [[Xénon]] Xe | ||
| + | *55 [[Césium]] Cs | ||
| + | *56 [[Baryum]] Ba | ||
| + | *57 [[Lanthane]] La | ||
| + | *58 [[Cérium]] Ce | ||
| + | *59 [[Praséodyme]] Pr | ||
| + | |width:25%| | ||
| + | | | ||
| + | *60 [[Néodyme]] Nd | ||
| + | *61 [[Prométhium]] Pm | ||
| + | *62 [[Samarium]] Sm | ||
| + | *63 [[Europium]] Eu | ||
| + | *64 [[Gadolinium]] Gd | ||
| + | *65 [[Terbium]] Tb | ||
| + | *66 [[Dysprosium]] Dy | ||
| + | *67 [[Holmium]] Ho | ||
| + | *68 [[Erbium]] Er | ||
| + | *69 [[Thulium]] Tm | ||
| + | *70 [[Ytterbium]] Yb | ||
| + | *71 [[Lutécium]] Lu | ||
| + | *72 [[Hafnium]] Hf | ||
| + | *73 [[Tantale]] Ta | ||
| + | *74 [[Tungstène]] W | ||
| + | *75 [[Rhénium]] Re | ||
| + | *76 [[Osmium]] Os | ||
| + | *77 [[Iridium]] Ir | ||
| + | *78 [[Platine]] Pt | ||
| + | *79 [[Or]] Au | ||
| + | *80 [[Mercure]] Hg | ||
| + | *81 [[Thallium]] Tl | ||
| + | *82 [[Plomb]] Pb | ||
| + | *83 [[Bismuth]] Bi | ||
| + | *84 [[Polonium]] Po | ||
| + | *85 [[Astate]] At | ||
| + | *86 [[Radon]] Rn | ||
| + | *87 [[Francium]] Fr | ||
| + | *88 [[Radium]] Ra | ||
| + | *89 [[Actinium]] Ac | ||
| + | |width:25%| | ||
| + | | | ||
| + | *90 [[Thorium]] Th | ||
| + | *91 [[Protactinium]] Pa | ||
| + | *92 [[Uranium]] U | ||
| + | *93 [[Neptunium]] Np | ||
| + | *94 [[Plutonium]] Pu | ||
| + | *95 Américium Am | ||
| + | *96 Curium Cm | ||
| + | *97 Berkélium Bk | ||
| + | *98 Californium Cf | ||
| + | *99 Einsteinium Es | ||
| + | *100 Fermium Fm | ||
| + | *101 Mendélévium Md | ||
| + | *102 Nobélium No | ||
| + | *103 Lawrencium Lr | ||
| + | *104 Rutherfordium Rf | ||
| + | *105 Dubnium Db | ||
| + | *106 Seaborgium Sg | ||
| + | *107 Bohrium Bh | ||
| + | *108 Hassium Hs | ||
| + | *109 Meitnérium Mt | ||
| + | *110 Darmstadtium Ds | ||
| + | *111 Roentgenium Rg | ||
| + | *112 Ununbium Uub | ||
| + | *113 Ununtrium Uut | ||
| + | *114 Ununquadium Uuq | ||
| + | *115 Ununpentium Uup | ||
| + | *116 Ununhexium Uuh | ||
| + | *117 Ununseptium Uus (#) | ||
| + | *118 Ununoctium Uuo | ||
| + | |} | ||
| + | </center> | ||
| + | On connait actuellement 118 éléments (du 1 au 118, [#] avec la découverte confirmée du 117, début 2010 ! ) dont 94 existent à l'état naturel sur [[Terre]], du 1 au 94, les suivants sont tous des [[éléments synthétiques]]. | ||
| + | *<b><font color="green">Il vous est possible de consulter une</font> [[Liste alphabétique des éléments naturels]],</b> avec leurs symboles et leurs séries. | ||
<hr> | <hr> | ||
| − | <font color=" | + | <font color="green">Retour aux différentes </font>[[listes]] |
<hr> | <hr> | ||
| − | < | + | <br clear="all" /> |
| + | {| align="center" class="toccolours" cellspacing="0" | ||
| + | |- bgcolor="#ccccff" | ||
| + | | align="center" | '''à voir aussi pour en apprendre plus sur les minéraux et les roches''' | ||
| + | |- | ||
| + | | align="center" style="font-size: 100%;" | [[Vocabulaire géologique]] | [[Lexique volcanologique]] | [[Liste alphabétique des éléments naturels]] | [[Lexique des termes employés en minéralogie]] | ||
| + | |- | ||
| + | | align="center" style="font-size: 100%;" | [[Minéraux]] | [[Liste des personnalités]] | ||
| + | |} | ||
Version actuelle datée du 6 mars 2021 à 09:32
- Pendant l'Antiquité, on considérait les éléments différemment : les corps étaient classés en solides, liquides et vapeurs et selon leur couleur, et leur interaction suivant des notions de sympathie et d'antipathie. Cette philosophie reposait sur la théorie des quatre éléments (le feu, l’eau, la terre et l’air) d'Aristote reprise par Platon. (Voir l'histoire de la chimie).
- Origine des éléments (Suivre le lien), à noter que les tout premiers éléments formés naturellement (Big Bang) se retrouvent en haut du tableau (ligne 1 : hydrogène et hélium), et les éléments synthétisés par l'homme (éléments synthétiques), sont en bas du tableau (voir le tableau ci-dessous).
- Les éléments chimiques sont une catégorie d'atomes ayants en commun le même nombre de protons dans leur noyau atomique. Un atome est un assemblage de protons, de charge positive, et de neutrons, de charge nulle, le tout entouré d'électrons de charge électrique négative. Les atomes peuvent se combiner de façons très variables. Sous forme pure, ils peuvent se présenter notamment : comme des atomes séparés, comme des molécules (comprenant plusieurs atomes d'un même élément), comme des solides cristallins (ou amorphes).

- Élément natif (adj.) du latin nativus, naturel : Qualifie les éléments chimiques métalliques qui se trouvent dans la nature à l'état pur (or, argent, cuivre, fer, chrome, aluminium, mercure, etc.). Certains des éléments natifs peuvent se combiner et constituer des " alliages " ou des " amalgames " naturels…
- Tableau périodique des éléments : ou tableau de Mendeleïev, regroupe tous les éléments avec, leur numéro atomique, la masse atomique, le nom, le symbole... Ce tableau est dit périodique car tous les éléments situés dans une même colonne (de 1 à 18), présentent des propriétés chimiques proches. Par exemple : dans la colonne 1, le lithium (Li) et le sodium (Na) ont un comportement chimique proche. L'explication de ce comportement repose sur le fait que le nombre d'électrons de leur couche de valence (tous les électrons présents en plus de la configuration du dernier gaz rare) est identique. Li et Na ont un seul électron de valence. C'est cet électron externe qui est disponible pour les réactions chimiques. D'où des propriétés chimiques proches et par conséquent leur regroupement dans une même famille d'éléments.
- Les éléments, (métaux, à gauche du tableau et non métaux, à droite du tableau) sont regroupés en dix séries chimiques aux propriétés physicochimiques homogènes :
- Série des métaux alcalins,
- Série des métaux alcalino-terreux,
- Série des lanthanides : Z = 57 à 71,
- Série des actinides : Z = 89 à 103,
- Série des métaux de transition (colonnes 3 à 12),
- Série des métaux pauvres entre les métalloïdes et les métaux de transition (Al, Ga, In, Sn, Tl, Pb, Bi),
- Série des métalloïdes : entre les deux précédents (B, Si, Ge, As, Sb, Te, Po),
- Série des non-métaux à droite du tableau :
- Série des halogènes : colonne 17,
- Série des gaz nobles : colonne 18.
- Chaque série correspondant à une couleur du tableau.
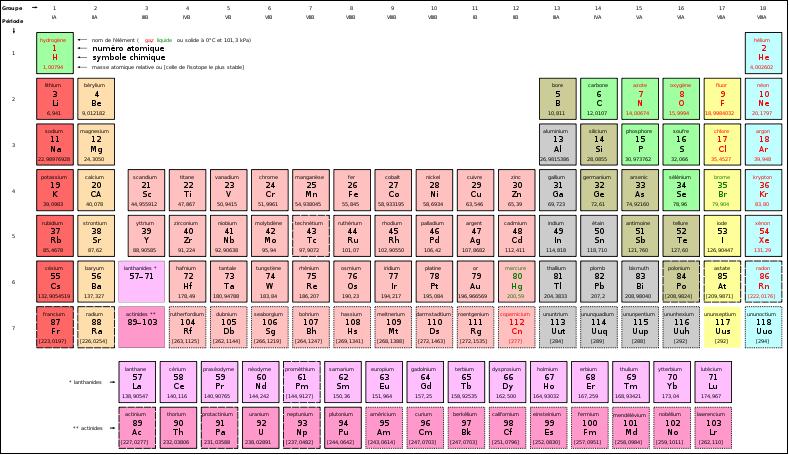
Pour voir le tableau en plus grand, voir : Le tableau des éléments
Une autre version (plus ancienne) du tableau périodique des éléments se trouve à : FORMULES CHIMIQUES et à Mendeleïev.
- Les éléments sont aussi placés dans des groupes, dont chacun a des propriétés bien distinctes de celles des groupes voisins. On distingue 18 groupes :
- groupe 1 des métaux alcalins
- groupe 2 des métaux alcalino-terreux
- groupe 14 des cristallogènes
- groupe 15 des pnictogènes
- groupe 16 des chalcogènes
- groupe 17 des halogènes
- groupe 18 des gaz rares
- + groupe des lanthanides et actinides
- + groupe du platine (ruthénium, rhodium, osmium, iridium et platine).
- + les terres rares
|
|
|
|
On connait actuellement 118 éléments (du 1 au 118, [#] avec la découverte confirmée du 117, début 2010 ! ) dont 94 existent à l'état naturel sur Terre, du 1 au 94, les suivants sont tous des éléments synthétiques.
- Il vous est possible de consulter une Liste alphabétique des éléments naturels, avec leurs symboles et leurs séries.
Retour aux différentes listes
| à voir aussi pour en apprendre plus sur les minéraux et les roches |
| Vocabulaire géologique | Lexique volcanologique | Liste alphabétique des éléments naturels | Lexique des termes employés en minéralogie |
| Minéraux | Liste des personnalités |