FORMULES CHIMIQUES : Différence entre versions
m |
|||
| Ligne 3 : | Ligne 3 : | ||
=====Atomes, ions et éléments===== | =====Atomes, ions et éléments===== | ||
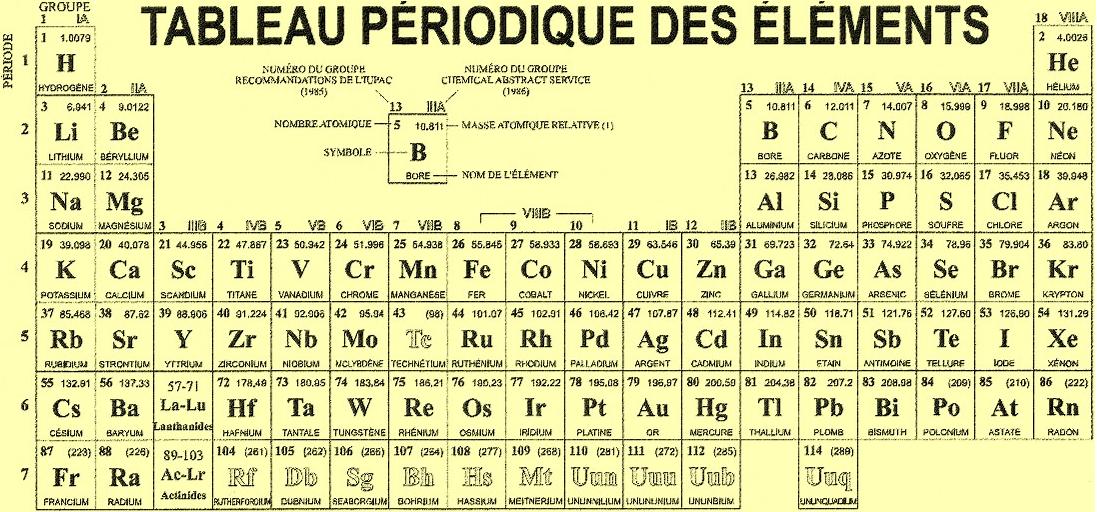
| − | *<b>les atomes</b> sont au nombre de 103 types, les 103 <b>éléments</b> (tableau périodique des éléments ). Chaque élément est désigné par un code d'une lettre capitale, ou de deux lettres | + | *<b>les atomes</b> sont au nombre de 103 types, les 103 <b>éléments</b> (tableau périodique des éléments). Chaque élément est désigné par un code d'une lettre capitale, ou de deux lettres dont la première est une capitale et la seconde une minuscule ; c'est le '''symbole chimique'''.<br> |
<center> [[Image:Masse_atomique2.jpg]]</center> | <center> [[Image:Masse_atomique2.jpg]]</center> | ||
Par exemple : l'hydrogène est désigné par '''H''', le carbone par '''C''', l'azote par '''N''' , l'oxygène par '''O''', le sodium par '''Na''' ), le fer par '''Fe''', le calcium par '''Ca''' ...<br> | Par exemple : l'hydrogène est désigné par '''H''', le carbone par '''C''', l'azote par '''N''' , l'oxygène par '''O''', le sodium par '''Na''' ), le fer par '''Fe''', le calcium par '''Ca''' ...<br> | ||
Si d'aventure un électron est arraché à l'atome, il y a une charge '''+e''' excédentaire, on a ce que l'on appelle un «ion positif» ou «cation».<br> | Si d'aventure un électron est arraché à l'atome, il y a une charge '''+e''' excédentaire, on a ce que l'on appelle un «ion positif» ou «cation».<br> | ||
Si par contre l'atome capture un électron qui passait par là, il y a une charge '''-e''' excédentaire, on a ce que l'on appelle un «ion négatif» ou «anion». <br> | Si par contre l'atome capture un électron qui passait par là, il y a une charge '''-e''' excédentaire, on a ce que l'on appelle un «ion négatif» ou «anion». <br> | ||
| − | Mais le noyau est inchangé, on a toujours le même élément chimique avec le même numéro | + | Mais le noyau est inchangé, on a toujours le même élément chimique avec le même numéro atomique.<br> |
*<b>Les ions</b> sont des atomes qui ont perdu ou gagné un ou plusieurs électrons ; il ne sont plus neutres électriquement. | *<b>Les ions</b> sont des atomes qui ont perdu ou gagné un ou plusieurs électrons ; il ne sont plus neutres électriquement. | ||
| Ligne 15 : | Ligne 15 : | ||
=====Liaison ionique===== | =====Liaison ionique===== | ||
| − | On sait que les objets ayant une charge opposée s'attirent, et les objets ayant une charge de même signe se repoussent. Les '''+''' se repoussent entre eux, | + | On sait que les objets ayant une charge opposée s'attirent, et que les objets ayant une charge de même signe se repoussent. Les '''+''' se repoussent entre eux, les '''-''' se repoussent entre eux, mais un '''+''' et un '''-''' s'attirent (force de Coulomb). Les ions se baladant dans la nature vont donc être attirés par des ions ayant une charge opposée, ils vont former un édifice électriquement neutre. Cette attraction électrostatique forme ce que l'on appelle la «liaison ionique». Elle est à l'origine de la cristallisation du sel.<br> |
| − | Ainsi, les ions sodium Na+ et les ions chlore Cl- s'associent pour former le chlorure de sodium NaCl (édifice neutre), qui n'est autre que le sel de cuisine. Les ions sont empilés en alternance, de sorte qu'un ion + n'est entouré que d'ions -, et un ion - n'est entouré que d'ions +. | + | Ainsi, les ions sodium Na+ et les ions chlore Cl- s'associent pour former le chlorure de sodium NaCl (édifice neutre), qui n'est autre que le sel de cuisine ([[halite]]). Les ions sont empilés en alternance, de sorte qu'un ion + n'est entouré que d'ions -, et un ion - n'est entouré que d'ions +. |
=====Liaison moléculaire===== | =====Liaison moléculaire===== | ||
| Ligne 26 : | Ligne 26 : | ||
=====Formules chimiques===== | =====Formules chimiques===== | ||
| − | <b>Les éléments</b> se combinent pour faire tous les minéraux et roches trouvés dans la croûte | + | <b>Les éléments</b> se combinent pour faire tous les minéraux et roches trouvés dans la croûte terrestre. Les huit éléments principaux sont : oxygène '''O''', silicium '''Si''', aluminium '''Al''', fer '''Fe''', calcium '''Ca''', sodium '''Na''', potassium '''K''', et magnésium '''Mg'''.<br> |
| − | Le silicium '''Si''' combine avec deux atomes de l'oxygène '''O<sub>2</sub>''' pour donner '''SiO<sub>2</sub>''' pour faire le [[quartz]], ou de la silice, et de | + | Le silicium '''Si''' combine avec deux atomes de l'oxygène '''O<sub>2</sub>''' pour donner '''SiO<sub>2</sub>''' pour faire le [[quartz]], ou de la silice, et de là tous les minéraux silicatés (voir à [[Silicates]]). |
Les mineraux peuvent être : | Les mineraux peuvent être : | ||
| Ligne 34 : | Ligne 34 : | ||
<b>Le point de départ est une analyse chimique</b>.<br> | <b>Le point de départ est une analyse chimique</b>.<br> | ||
| − | La composition définie indique qu'une analyse chimique d'un minéral donné produira toujours le même taux des éléments. Par exemple, le quartz aura toujours un silicium '''Si''' pour chaque deux atomes d'oxygène '''O<sub>2</sub>'''. Par conséquent, les mineraux peuvent être exprimés par des formules chimiques, telles que SiO<sub>2</sub> pour le quartz. | + | La composition définie indique qu'une analyse chimique d'un minéral donné produira toujours le même taux des éléments. Par exemple, le quartz aura toujours un silicium '''Si''' pour chaque (groupe de) deux atomes d'oxygène '''O<sub>2</sub>'''. Par conséquent, les mineraux peuvent être exprimés par des formules chimiques, telles que SiO<sub>2</sub> pour le quartz. |
| − | Dans certains minéraux, les éléments sont de taille et de charge semblable, ils se remplacent l'un l'autre. La quantité de fer et magnésium dans l'olivine change parce que ces éléments peuvent se remplacer l'un l'autre dans la structure du minéral. La formule de l’olivine, qui est un nom général pour un mélange (une solution solide) entre deux pôles principaux, la | + | Dans certains minéraux, les éléments sont de taille et de charge semblable, ils se remplacent l'un l'autre. La quantité de fer et magnésium dans l'olivine change parce que ces éléments peuvent se remplacer l'un l'autre dans la structure du minéral. La formule de l’olivine, qui est un nom général pour un mélange (une solution solide) entre deux pôles principaux, la forstérite '''MgSiO<sub>4</sub>''' et la fayalite '''FeSiO<sub>4</sub>''', indique que pour chaque (groupe de) deux atomes de magnésium et/ou de fer, il y a un atome de silicium et quatre atomes d'oxygène.<br> |
Généralement, une formule d’[[olivine]] est écrite '''(Mg,Fe)<sub>2</sub>SiO<sub>4</sub>'''. | Généralement, une formule d’[[olivine]] est écrite '''(Mg,Fe)<sub>2</sub>SiO<sub>4</sub>'''. | ||
| Ligne 49 : | Ligne 49 : | ||
|} | |} | ||
<font color="#0000FF">Retour à </font>[[Lexique des termes employés en minéralogie]] | <font color="#0000FF">Retour à </font>[[Lexique des termes employés en minéralogie]] | ||
| + | <hr> | ||
| + | <font color="#0000FF">Retour à</font> [[Liste alphabétique des éléments naturels]] | ||
Version du 25 juin 2009 à 14:53
Sommaire
Composition chimique
Les minéraux ont une composition chimique bien déterminée, exprimée par une formule chimique. Cette formule est idéalisée, c'est-à-dire qu'elle ne mentionne que les principaux composants du minéral. Les très petites inclusions ou impuretés naturelles, qui peuvent influencer la couleur ou même la faire changer, ne sont pas prises en compte.
Atomes, ions et éléments
- les atomes sont au nombre de 103 types, les 103 éléments (tableau périodique des éléments). Chaque élément est désigné par un code d'une lettre capitale, ou de deux lettres dont la première est une capitale et la seconde une minuscule ; c'est le symbole chimique.
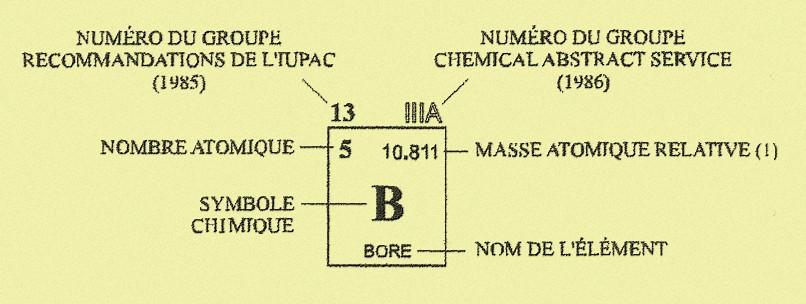
Par exemple : l'hydrogène est désigné par H, le carbone par C, l'azote par N , l'oxygène par O, le sodium par Na ), le fer par Fe, le calcium par Ca ...
Si d'aventure un électron est arraché à l'atome, il y a une charge +e excédentaire, on a ce que l'on appelle un «ion positif» ou «cation».
Si par contre l'atome capture un électron qui passait par là, il y a une charge -e excédentaire, on a ce que l'on appelle un «ion négatif» ou «anion».
Mais le noyau est inchangé, on a toujours le même élément chimique avec le même numéro atomique.
- Les ions sont des atomes qui ont perdu ou gagné un ou plusieurs électrons ; il ne sont plus neutres électriquement.
Liaison ionique
On sait que les objets ayant une charge opposée s'attirent, et que les objets ayant une charge de même signe se repoussent. Les + se repoussent entre eux, les - se repoussent entre eux, mais un + et un - s'attirent (force de Coulomb). Les ions se baladant dans la nature vont donc être attirés par des ions ayant une charge opposée, ils vont former un édifice électriquement neutre. Cette attraction électrostatique forme ce que l'on appelle la «liaison ionique». Elle est à l'origine de la cristallisation du sel.
Ainsi, les ions sodium Na+ et les ions chlore Cl- s'associent pour former le chlorure de sodium NaCl (édifice neutre), qui n'est autre que le sel de cuisine (halite). Les ions sont empilés en alternance, de sorte qu'un ion + n'est entouré que d'ions -, et un ion - n'est entouré que d'ions +.
Liaison moléculaire
Plutôt que de voler un électron à un autre atome comme dans le cas d'une réaction électrochimique, il peut y avoir une mise en commun d'un électron (chaque atome apporte un électron qu'il partage avec l'autre atome). C'est la liaison moléculaire ou liaison covalente.
- Les deux atomes peuvent être identiques, alors, on met un2 en indice du symbole chimique pour indiquer que la molécule contient deux atomes identiques : p.ex. les gaz dihydrogène H2, dioxygène O2.
- Les atomes peuvent aussi être différents, on accole alors les deux symboles chimiques : p.ex. le monoxyde de carbone CO, le chlorure d'hydrogène HCl.
Un atome peut partager ses électrons avec plusieurs autres atomes, le carbone peut ainsi partager jusqu'à 4 électrons. Dans le cas de l'eau, l'atome d'oxygène partage deux électrons, un avec chaque atome d'hydrogène : H2O.
Formules chimiques
Les éléments se combinent pour faire tous les minéraux et roches trouvés dans la croûte terrestre. Les huit éléments principaux sont : oxygène O, silicium Si, aluminium Al, fer Fe, calcium Ca, sodium Na, potassium K, et magnésium Mg.
Le silicium Si combine avec deux atomes de l'oxygène O2 pour donner SiO2 pour faire le quartz, ou de la silice, et de là tous les minéraux silicatés (voir à Silicates).
Les mineraux peuvent être :
- un élément simple, comme le diamant, qui est fait de carbone C, formule chimique : C
- des composés de deux éléments ou plus, comme le quartz, qui contient un silicium Si et deux atomes d'oxygène O2, formule chimique : SiO2.
Le point de départ est une analyse chimique.
La composition définie indique qu'une analyse chimique d'un minéral donné produira toujours le même taux des éléments. Par exemple, le quartz aura toujours un silicium Si pour chaque (groupe de) deux atomes d'oxygène O2. Par conséquent, les mineraux peuvent être exprimés par des formules chimiques, telles que SiO2 pour le quartz.
Dans certains minéraux, les éléments sont de taille et de charge semblable, ils se remplacent l'un l'autre. La quantité de fer et magnésium dans l'olivine change parce que ces éléments peuvent se remplacer l'un l'autre dans la structure du minéral. La formule de l’olivine, qui est un nom général pour un mélange (une solution solide) entre deux pôles principaux, la forstérite MgSiO4 et la fayalite FeSiO4, indique que pour chaque (groupe de) deux atomes de magnésium et/ou de fer, il y a un atome de silicium et quatre atomes d'oxygène.
Généralement, une formule d’olivine est écrite (Mg,Fe)2SiO4.
FORMULES CHIMIQUES des PRINCIPAUX MINERAUX

|

|

|
Retour à Lexique des termes employés en minéralogie